Серная кислота – двухосновная субстанция, являющаяся одной из самых опасных, высоко токсичных и самых едких химических реагентов. Особенно касается это концентрированных жидкостей. Но даже при таких характеристиках данная кислота в ряде случаев является высоко востребованным и незаменимым химическим веществом, без которого не было бы многих удобрений, лекарственных препаратов, средств очищение нефтепродуктов, различной химической и другой продукции.
Товары
В наличии
В наличии
В наличии
Свойства и характеристики серной кислоты
Чистая серная кислота являет собой вязкую едкую маслянистую жидкость без цвета и запаха с выраженным медным вкусом, которая при температуре 10,4° С превращается в кристаллическую твердую субстанцию. Концентрированный раствор (выше 40%) легко реагирует с водой, в результате чего образуются гидраты и выделяется большое количество тепла.
Благодаря высокой гигроскопичности реагент хорошо поглощает из воздуха водные пары. За счет этой способности может использоваться для осушения газов, которые не реагируют с кислотой.
В концентрированном виде раствор является мощным окислителем. Разбавленный реагент не обладает окислительными свойствами, взаимодействует с расположенными слева от водорода в электрохимическом ряду металлами.
Сферы применения
В жизнедеятельности человека серная кислота применяется в многих производственных направлениях – в производстве пластмасс, изготовлении красок, моющих средств и других материалов. Но основное применение серной кислоты приходится на производство разнообразных минеральных удобрений.
С недавних пор серную кислоту активно начали использовать при сборе картофеля. Реагент высушивает и останавливает рост побегов, расщепляя при этом значительную часть почвы и упрощая процесс сбора урожая машинным способом.
Около 200 млн. тонн ежегодно составляет потребление человечеством серной кислоты для самых различных нужд. Рассмотрим более подробно в каких направлениях и для чего используют едкий и в многих случаях смертельно опасный реагент.

Серная кислота в промышленности
Серная кислота активно применяется в различных областях промышленности. За счет постоянного спроса этот химический реагент называют «едкой кровью» промышленности. С раствором работают инженеры и ученые, ученики и студенты. Без данной кислоты трудно представить функционирование современной экономики.
Если выделить только основные области применения серной кислоты на производственных объектах, то в этом направлении стоит отметить следующие:
- производство удобрений составляет наибольший расход H2SO4. Востребована кислота в изготовлении различных суперфосфатов, сульфата и фосфата аммония;
- в черной металлургии жидкость с помощью жидкости эффективно и легко очищают от окалины, ржавчины и оксидной пленки проволоки, разные заготовки и листовой металлопрокат перед их цинкованием. Также продукт эффективен в травлении металлов перед их покрытием никелем, хромом, медью и другими материалами;
- в цветной металлургии раствор задействуют при получении цветных металлов, а также как средство для восстановления алюминия;
- в пищевой промышленности H2SO4 выполняет роль эмульгатора и употребляется в виде пищевой добавки Е513, которая регулирует кислотность разнообразных напитков;
- в целлюлозно-бумажной отрасли раствор используют в изготовлении тканей и бумаги с цветным покрытием, в получении целлофана, ацетата, вискозы и капролактама. Нередко задействуют в качестве средства для проклейки бумаги;
- в добывающей промышленности с помощью кислоты из разных видов руд выделяют редкоземельные элементы.
Промышленный органический синтез невозможно представить без серной кислоты. Она активно задействуется в реакциях гидратации, дегидратации и алкилирования. Изготовление эмалей, красок, чернил и различных пигментов, получение разных неорганических соединений (борной, соляной, фосфорной и других кислот), синтез органических веществ (анилиновых красителей, сложных эфиров, моющих средств, синтетических смол, лекарственных средств) – в этих и многих других целях серная кислота активно задействуется.
Серная кислота в быту
H2SO4 входит в состав средств, используемых для очистки водопроводных труб. Жидкость отлично решает задачи устранения заторов в системах водоснабжения и очистки воды.
Также в бытовых условиях повышенным спросом среди автовладельцев пользуется аккумуляторная серная кислота. Она добавляется к электролиту для свинцовых автомобильных аккумуляторов.
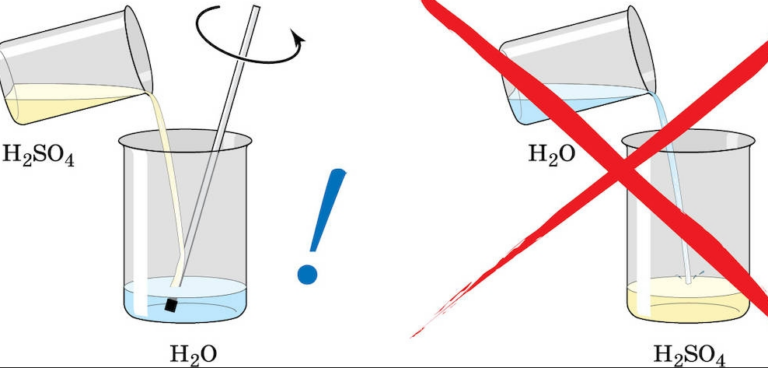
Крайне важно при работе с кислотой соблюдать правила безопасности. При заправке аккумулятора нужно кислоту к воде добавлять постепенно, но ни в коем случае не наоборот. Поскольку при вступлении в реакцию с раствором вода сильно нагревается, что может спровоцировать ее разбрызгивание. Если жидкость попадет на лицо или в глаза, то это чревато ожогами.
Разлитая на металл кислота хорошо нейтрализуется с помощью мела или извести. При попадании реактива на одежду ее нужно снять. В случае попадания жидкости на кожу необходимо сразу же тщательно промыть пораженные места чистой проточной водой.
Хранить раствор следует в закрытой герметической емкости в месте, недоступном для детей.

Серная кислота в сельском хозяйстве
Сельскохозяйственная отрасль – еще одна область применения серной кислоты. Из нее изготавливают различные ядохимикаты, используемые для борьбы с сорными травами и вредителями культур.
Соли и разбавленные растворы серной кислоты применяют:
- для дезинфекции овощехранилищ, оранжерей, теплиц и парников;
- в качестве средства для предотвращения образования плесени и грибков;
- для борьбы с различными вредителями и противодействия разным видам клещей;
- как средство для борьбы с болезнями, в частности для предотвращения корневой гнили и противодействия появления мучнистой росы на плодовых деревьях, виноградниках и хлопчатниковых плантациях;
- для удобрения растений. Сера укрепляет корневую систему и ускоряет процесс усвоения растениями микроэлементов.
Для повышения кислотности почвы жидкая сера является самым простым и быстрым решением. Вносить ее можно непосредственно в грунт.
Серная кислота в медицине
Широкое применение серная кислота нашла также в медицине. В этом направлении высоким спросом пользуются ее соли.
Известным производным реагента является натрий тиосульфат, который задействуется в качестве противоядия при отравлении свинцом, ртутью, цианидом или галогенами. Также препарат эффективен в лечении разных дерматологических заболеваний.
В виде действенного спазмолитика больным гипертоническими болезнями вводят магний сульфат – производное серной кислоты. Этот же препарат назначают людям с проблемами желчеотделения.
Гинекологи используют магния сульфат для обезболивания родов методом внутримышечного введения. Также препарат известен как эффективное антисудорожное средство.
Биологическая опасность серной кислоты и особенности ее применения
Независимо для каких целей используется серная кислота применение ее требует строгого соблюдения правил безопасности. По уровню токсичности жидкость принадлежит ко 2 классу опасности. Испаряемые раствором пары поражают слизистые оболочки, кожу, дыхательные пути, вызывая рвоту, отравления, затруднение дыхания и тяжелые химические ожоги.
Поэтому работать с жидкостью необходимо предельно осторожно, обязательно используя средства личной защиты и спецодежду.
В процессе приготовления электролита категорически нельзя в серную кислоту вливать воду, поскольку это чревато поражениями кожи, глаз и других органов. Электролит перед заливкой в аккумулятор обязательно следует охладить как минимум до 25° С. Хранить состав нужно в плотно закрытой керамической, фаянсовой или эбонитовой посуде, но ни в коем случае не в металлической.
Для хранения серной кислоты в больших объемах на производственных предприятиях нужно применять специализированные емкости, оснащенные смотровыми окнами, датчиками контроля и надежной запорной арматурой.
Поэтому работать с кислотой необходимо в маске и очках. Если кислота используется внутри помещений, то в нем обязательно должна быть вытяжка, способная быстро выводить едкие пары.
Всегда нужно помнить о том, что любое неосторожное обращение с кислотой может повлечь за собой серьезные проблемы со здоровьем, в том числе опасность для жизни.
Читайте также
Сертификаты и паспорта поставляемой продукции



